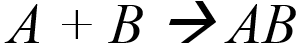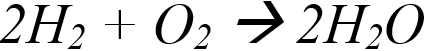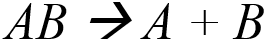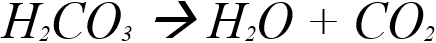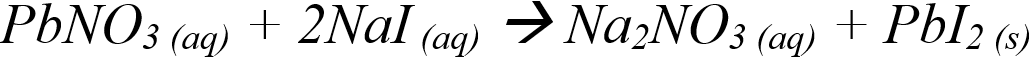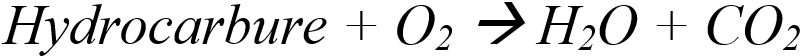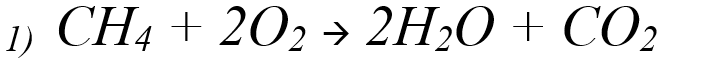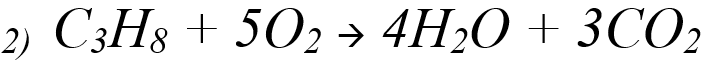Liste des résultats d'apprentissage
L’élève sera apte à :
L’élève sera apte à :
- équilibrer des équations chimiques, entre autres traduire en mots des équations chimiques équilibrées, et traduire en équations chimiques équilibrées des équations exprimées en mots;
- étudier la loi de la conservation de la masse et reconnaître que la masse se conserve au cours des réactions chimiques;
- étudier des réactions chimiques et les classer selon qu'il s'agit d'une synthèse, d'une décomposition, d'un déplacement simple, d'un déplacement double ou d'une combustion;
Masse des composés et conservation de la masse
Dans une réaction chimique, des substances (les réactifs) changent leurs structures chimiques pour devenir des substances différentes (les produits). La loi de la conservation de la masse énonce que la masse totale des réactifs est égale à la masse totale des produits. Ceci signifie que toute la matière des réactifs se retrouve complètement dans les produits. Il n'y a pas de nouvelle matière qui s'ajoute ou de matière qui disparaît. La matière ne fait que créer des liaisons différentes. Pour vérifier cette loi, il faut pouvoir mesurer avec précision la masse des réactifs et celle de tous les produits.
Masse d'un composé
Le tableau périodique des éléments nous renseigne sur la masse atomique de chaque élément. Les masses atomiques y sont données en unités de masse atomique (uma). Par exemple, la masse d'un atome de carbone est de 12,01 uma et celle d'un atome d'oxygène est de 16,00 uma (ces masses sont arrondies). Ces deux atomes peuvent s'associer entre eux pour former du monoxyde de carbone (CO). Puisqu'il y a un atome de carbone et un atome d'oxygène dans le monoxyde de carbone, une molécule de monoxyde de carbone possède une masse de 28,01 uma (soit 12,01 uma + 16,00 uma).
Masse d'un composé
Le tableau périodique des éléments nous renseigne sur la masse atomique de chaque élément. Les masses atomiques y sont données en unités de masse atomique (uma). Par exemple, la masse d'un atome de carbone est de 12,01 uma et celle d'un atome d'oxygène est de 16,00 uma (ces masses sont arrondies). Ces deux atomes peuvent s'associer entre eux pour former du monoxyde de carbone (CO). Puisqu'il y a un atome de carbone et un atome d'oxygène dans le monoxyde de carbone, une molécule de monoxyde de carbone possède une masse de 28,01 uma (soit 12,01 uma + 16,00 uma).
Voici d'autres exemples de masses de composés calculées à partir de la masse atomique des atomes qui les composent.
Équation chimique
Une équation chimique représente une réaction chimique. Le mot « équation » indique bien que tous les termes à gauche de l'équation doivent se retrouver en part égale à droite de l'équation. Toutefois, contrairement à une équation mathématiques, on ne peut pas nécessairement inverser les côtés de l'équation : en mathématiques, si A = B, on conclut que B = A. Dans une équation chimique, on n'utilise pas le symbole d'égalité, mais une flèche qui indique le sens de la réaction : A -> B signifie que les réactifs (représentés par A) réagissent pour former les produits (représentés par B). Cette réaction n'est pas forcément possible dans l'autre sens et si A -> B, on ne peut pas affirmer que B -> A.
Voici un exemple d'une équation représentant la réaction entre le magnésium et l'acide chlorhydrique qui produit de l'hydrogène gazeux et du chlorure de magnésium.
Dans cette équation, on remarque que
Équilibrer une équation (par tâtonnement)
- Chaque atome de magnésium réagit avec deux molécules d'acide chlorhydrique pour produire du dihydrogène gazeux et du chlorure de magnésium en solution aqueuse (équation exprimée en mots).
- Les réactifs sont à gauche de l'équation et les produits sont à droite tel qu'indiqué par le sens de la flèche.
- Il y a un coefficient devant le second terme (2 HCl) de manière à ce qu'on retrouve tous les atomes de gauche à droite, dans les mêmes quantités (1 atome de magnésium, 2 atomes d'hydrogène et 2 atomes de chlore de chaque côté). On dit que l'équation est équilibrée.
- Les symbole (g), (s) et (aq) représentent l'état dans lequel les composés se trouvent. Le magnésium est solide (s), le chlorure d'hydrogène est dilué dans de l'eau, il est en solution aqueuse (aq), lui procurant ses propriétés acides : on lui donne ainsi le nom d'acide chlorhydrique. Le dihydrogène apparaît sous forme de gaz (g) et le chlorure de magnésium est aussi dissout dans l'eau (aq). Ces symboles ne sont pas obligatoires.
- On pourrait trouver la masse de chaque composé de l'équation et montrer que la somme des masses des réactifs est la même que la somme des masses des produits (soit 97,23 uma de chaque côté). Les équations équilibrées respectent la loi de conservation de la masse.
Équilibrer une équation (par tâtonnement)
- Écrire l'équation bilan (l'équation non-équilibrée)
- Compter le nombre d'atome de chaque élément de chaque côté de l'équation
- Équilibrer en premier l'élément qui se trouve dans un seul composé de chaque côté de l'équation. en ajoutant des coefficients devant les formules des composés. Généralement, on commence par les éléments les plus électronégatifs.
- multiplier les autres atomes par le nouveau coefficient et équilibrer de l'autre côté de l'équation
- Si on est forcé de diviser un atome en demi, multiplier tous les coefficients par 2.
- À la fin, tous les coefficients devraient être simplifiés, c'est à dire qu'il ne peut pas y avoir de diviseur commun autre que 1 à tous les coefficients.
|
|
|
Stœchiométrie
(Les notions de stœchiométrie ne font pas partie du programme d'étude de dixième année, mais permette une compréhension plus profonde du concept de conservation de la masse)
La stœchiométrie est l'utilisation de la loi de conservation de la masse pour calculer les masses des composés dans une réactions chimique. La stœchiométrie est donc une méthode qui permet de prévoir la masses des produits lorsqu'on connaît l'équation de la réaction chimique ainsi que la masse des réactifs. Pour comprendre la stœchiométrie, il faut comprendre le concept de mole et de masse molaire.
Mole et masse molaire
En 1811, un scientifique italien du nom d'Amadeo Avogadro a constaté que des volumes égaux de gaz, soumis aux mêmes conditions de température et pression, contiennent les mêmes quantités de molécules. 50 ans plus tard, l'autrichien Johann Joseph Loschmidt calcule de manière imprécise le nombre de Loschmidt (qui sera rebaptisé nombre d'Avogadro par le français Jean Perrin en 1908) correspondant au nombre de molécules de gaz permettant de transformer en unité de grammes la masse moléculaire du gaz.
(Les notions de stœchiométrie ne font pas partie du programme d'étude de dixième année, mais permette une compréhension plus profonde du concept de conservation de la masse)
La stœchiométrie est l'utilisation de la loi de conservation de la masse pour calculer les masses des composés dans une réactions chimique. La stœchiométrie est donc une méthode qui permet de prévoir la masses des produits lorsqu'on connaît l'équation de la réaction chimique ainsi que la masse des réactifs. Pour comprendre la stœchiométrie, il faut comprendre le concept de mole et de masse molaire.
Mole et masse molaire
En 1811, un scientifique italien du nom d'Amadeo Avogadro a constaté que des volumes égaux de gaz, soumis aux mêmes conditions de température et pression, contiennent les mêmes quantités de molécules. 50 ans plus tard, l'autrichien Johann Joseph Loschmidt calcule de manière imprécise le nombre de Loschmidt (qui sera rebaptisé nombre d'Avogadro par le français Jean Perrin en 1908) correspondant au nombre de molécules de gaz permettant de transformer en unité de grammes la masse moléculaire du gaz.
Aujourd'hui, ce nombre est estimé à 6,0221367 X 1023 molécules. Ceci signifie, par exemple, qu'il faut 6,0221367 x 1023 molécules d'oxygène (O2), dont la masse moléculaire est de 32 uma (2 X 16 uma) pour avoir 32 grammes d'oxygène. On dit alors qu'une mole d'oxygène est de 32 g ou que la masse molaire de O2 = 32 g.
Le nombre d'Avogadro ne s'applique pas seulement aux gaz, mais à toute molécule et atome. Ainsi, une mole de fer possède une masse de 55,85 g et une mole d'argent a une masse de 107,87 g.
Application
L'exemple suivant illustre comment utiliser les concepts de stœchiométrie et de mole pour prévoir les masses des produits d'une réaction chimique.
Problème : On veut savoir combien d'hydrogène sera produit si 10g de magnésium réagissent complètement dans de l'acide chlorhydrique. On veut connaître aussi la quantité d'acide qui a réagit.
1) Poser l'équation équilibrée de la réaction chimique
Application
L'exemple suivant illustre comment utiliser les concepts de stœchiométrie et de mole pour prévoir les masses des produits d'une réaction chimique.
Problème : On veut savoir combien d'hydrogène sera produit si 10g de magnésium réagissent complètement dans de l'acide chlorhydrique. On veut connaître aussi la quantité d'acide qui a réagit.
1) Poser l'équation équilibrée de la réaction chimique
2) Trouver le nombre de mole de magnésium correspondant à 10g.
3) Déduire le nombre de mole de chaque terme selon le coefficient du terme. Puisqu'il y a deux molécules d'acide chlorhydrique pour chaque atome de magnésium (le coefficient de HCl est 2 et le coefficient de Mg est 1), Il y a deux moles d'acide chlorhydrique par mole de Mg. Comme il y a 0,41135 mole de Mg, on a besoin de 0,82271 moles de HCl. Avec la même logique, on conclue que la réaction produira 0,41135 moles de dihydrogène et de chlorure de magnésium.
Ce résultat constitue une solution complète au problème de départ : Il faut 0,823 mole d'acide chlorhydrique pour faire réagir complètement 10g de magnésium. la réaction produira 0,411 mole de dihydrogène. Toutefois, il peut être plus pratique de connaître la masse en grammes.
4) Transcrire en grammes le nombre de moles de chaque terme.
Ce résultat constitue une solution complète au problème de départ : Il faut 0,823 mole d'acide chlorhydrique pour faire réagir complètement 10g de magnésium. la réaction produira 0,411 mole de dihydrogène. Toutefois, il peut être plus pratique de connaître la masse en grammes.
4) Transcrire en grammes le nombre de moles de chaque terme.
Incidemment, on peut calculer la masse du dernier terme de la réaction, le chlorure de magnésium, à 39,1648 g et démontrer le respect de la loi de conservation de la masse.
10 g de magnésium réagissent avec 29,996 g d'acide chlorhydrique pour produire 0,8292 g d'hydrogène et 39,1648 g de chlorure de magnésium. 40 g de réactifs produit 40 g de produits.
limite de la réaction
Si on reprend l'exemple précédent dans un contexte de laboratoire, on pourrait avoir le protocole suivant :
Toutefois, dans cette situation, il manquera d'acide chlorhydrique (HCl) pour réagir avec tout le magnésium. On dit alors que HCl est le terme limitatif de la réaction ou que HCl est le réactif limitant ou encore que la réaction est limitée par le HCl. Il n'y aura que 0,06 mole (la moitié de 0,12 mole) de magnésium qui réagira, soit 1,46 g. même si on utilise 10 g de magnésium et 4,38 g d'acide chlorhydrique, la masse totale des réactifs est alors de 5,84 g (4,38 g de HCl + 1,46 g de Mg) car 8,54 g de magnésium ne réagira pas. La masse totale de dihydrogène et de chlorure de magnésium produits sera donc de 5,84 g.
Pour qu'une réaction soit non limitée (réaction totale), il faut que toute la masse des réactifs réagisse. En pratique, les réactions chimiques sont rarement complètes. Le rendement d'une réaction chimique peut être calculée en divisant la masse de produit obtenue par la masse de produit calculée de manière théorique (voir le calcul de rendement sur lachimie.fr)
limite de la réaction
Si on reprend l'exemple précédent dans un contexte de laboratoire, on pourrait avoir le protocole suivant :
- Dans un bécher de 100 ml, verser 10 ml d'acide chlorhydrique 12 molaire. (Ceci signifie une concentration de 12 mol de HCL par litre de solution. puisqu'il n'y a que 10 ml, il n'y a donc que 0,12 moles de HCl.
- déposer 10 g de magnésium dans l'acide.
Toutefois, dans cette situation, il manquera d'acide chlorhydrique (HCl) pour réagir avec tout le magnésium. On dit alors que HCl est le terme limitatif de la réaction ou que HCl est le réactif limitant ou encore que la réaction est limitée par le HCl. Il n'y aura que 0,06 mole (la moitié de 0,12 mole) de magnésium qui réagira, soit 1,46 g. même si on utilise 10 g de magnésium et 4,38 g d'acide chlorhydrique, la masse totale des réactifs est alors de 5,84 g (4,38 g de HCl + 1,46 g de Mg) car 8,54 g de magnésium ne réagira pas. La masse totale de dihydrogène et de chlorure de magnésium produits sera donc de 5,84 g.
Pour qu'une réaction soit non limitée (réaction totale), il faut que toute la masse des réactifs réagisse. En pratique, les réactions chimiques sont rarement complètes. Le rendement d'une réaction chimique peut être calculée en divisant la masse de produit obtenue par la masse de produit calculée de manière théorique (voir le calcul de rendement sur lachimie.fr)
Classification des réactions chimiques
Pour prévoir les produits d'une réaction, les scientifiques ont classifié les réactions selon différents types suivant des patrons. Généralement, les réactions ont lieu entre des atomes d'éléments.
Les réactions chimiques provoque des changements observables qu'on appelle les indices de réactions chimiques. Parmi ces indices, on note des changements de température ou de couleur, l'apparition d'un gaz ou d'un précipité, ainsi que la production de lumière.
Synthèse
La synthèse est une réaction où deux atomes se lient entre eux pour former un composé. La synthèse peut être représenté par l'équation :
- qui peuvent compléter leurs couches de valence
- qui sont plus réactifs que les atomes des éléments avec lesquels les atomes sont déjà liés. Les scientifiques mesure la réactivité des éléments par un indice d'électronégativité. Cet indice indique à quel point un atome attire les électrons et donc à quel point il est agressif dans sa quête pour obtenir des électrons ou dans sa volonté de s'en départir. En règle général, plus le rayon atomique est grand, moins le noyau attire les électrons. Les plus gros métaux seront donc plus réactif que les plus petits métaux car il laisseront partir leurs électrons de valence plus facilement. À l'inverse, plus le rayon atomique est petit et plus les atomes attirent les électrons. Les non-métaux plus petits auront donc tendance à être plus réactifs que les plus gros non-métaux car ils attirent les électrons plus fortement. De plus, un atome qui n'a besoin que d'un seul électron pour compléter sa couche de valence sera plus réactif. En suivant ces règles, on peut conclure que les éléments les plus réactifs sont le fluor chez les non-métaux (petit rayon et besoin d'un seul électron de valence) et le francium pour les métaux (gros atome avec un seul électron à perdre). Les indices d'électronégativité se trouve sur certains tableaux périodiques.
Les réactions chimiques provoque des changements observables qu'on appelle les indices de réactions chimiques. Parmi ces indices, on note des changements de température ou de couleur, l'apparition d'un gaz ou d'un précipité, ainsi que la production de lumière.
Synthèse
La synthèse est une réaction où deux atomes se lient entre eux pour former un composé. La synthèse peut être représenté par l'équation :
Dans cet équation l'atome de l'élément A se lie avec l'atome de l'élément B pour former le composé AB. AB peut être une liaison ionique où A est un métal et B est un non-métal. Si AB est covalent, B est plus électronégatif que A.
Exemple de réaction de synthèse : synthèse de l'eau par réaction du dihydrogène qui explose en présence de dioxygène. Cette réaction produit de la chaleur et de la lumière. En raison de cette chaleur, l'eau produite est sous forme de vapeur.
Exemple de réaction de synthèse : synthèse de l'eau par réaction du dihydrogène qui explose en présence de dioxygène. Cette réaction produit de la chaleur et de la lumière. En raison de cette chaleur, l'eau produite est sous forme de vapeur.
Décomposition
La décomposition est le processus inverse de la synthèse. Lors d'une décomposition, les parties d'un composé se dissocient, souvent sous l'effet d'énergie, pour former des composés plus simples ou des éléments purs. On peut résumer la décomposition par l'équation :
AB est un composé. Sous l'effet d'une force énergétique, le composé se dissocie pour former des parties plus simples A et B.
Exemple de réaction de décomposition : Sous l'effet de chaleur, l'acide carbonique (qui donne le goût piquant aux boissons gazeuses) se décompose en eau et en gaz carbonique (les bulles des boissons gazeuses).
Exemple de réaction de décomposition : Sous l'effet de chaleur, l'acide carbonique (qui donne le goût piquant aux boissons gazeuses) se décompose en eau et en gaz carbonique (les bulles des boissons gazeuses).
Le dioxyde de carbone se dissout dans l'eau à basse température. À mesure que la température monte, plus de gaz carbonique est libéré par l'acide carbonique et moins ce gaz reste dissout dans la solution.
Déplacement simple
Le déplacement simple a lieu lorsqu'un atome d'un élément réagit avec un composé en prenant la place d'un des atomes dans ce composé. L'atome en déplace un autre dans le composé. On peut représenté ce type de réaction par l'équation :
Dans cet équation, A déplace B pour se lier à C. A est donc plus réactif que B. A et B pourraient être des métaux et C un non-métal.
Exemple de réaction de déplacement simple : réaction du magnésium et de l'acide chlorhydrique. Dans cette réaction, l'hydrogène est déplacé par le magnésium qui se lie au chlore (chlorure de magnésium en solution). L'hydrogène est libéré sous forme de bulles de dihydrogène gazeux.
Exemple de réaction de déplacement simple : réaction du magnésium et de l'acide chlorhydrique. Dans cette réaction, l'hydrogène est déplacé par le magnésium qui se lie au chlore (chlorure de magnésium en solution). L'hydrogène est libéré sous forme de bulles de dihydrogène gazeux.
Déplacement double
Le déplacement double a lieu quand des atomes sont échangés entre deux composés. On peut représenter ce type de réaction par l'équation :
L'atome A et C s'échangent de position. A se lie avec D et C avec B. Si A et C sont des métaux, B et D sont des non-métaux.
Exemple de réaction de déplacement double : Une solution de nitrate de plomb (II) réagit dans une solution d'iodure de sodium pour former un précipité jaune vif dans l'expérience appelée la pluie d'or.
Exemple de réaction de déplacement double : Une solution de nitrate de plomb (II) réagit dans une solution d'iodure de sodium pour former un précipité jaune vif dans l'expérience appelée la pluie d'or.
Le plomb et l'iode se sont pas autant réactifs que le sodium et l'ion nitrate qui se lient ensemble pour former le nitrate de sodium, un composé soluble qui demeure en solution. Le plomb et l'iode sont libérés et se lient pour former un composé insoluble qui se précipite en flocons solide jaune vif, donnant l'impression d'une pluie d'or.
Combustion
Une combustion complète est la réaction d'un hydrocarbure dans de l'oxygène pour produire de l'eau et du dioxyde de carbone. la combustion est complète lorsque l'hydrocarbure est en présence de suffisamment d'oxygène. Un hydrocarbure est un un groupe de composés, comme le nom l'indique contenant des atomes d'hydrogène et de carbone. Parmi les hydrocarbures, nous entendons souvent parlé de méthane (gaz à effet de serre), le butane (essence à briquet), le propane (carburant commun des BBQ) et l'octane (carburant des automobiles). La formule générale d'une combustion complète suit l'équation :
Combustion
Une combustion complète est la réaction d'un hydrocarbure dans de l'oxygène pour produire de l'eau et du dioxyde de carbone. la combustion est complète lorsque l'hydrocarbure est en présence de suffisamment d'oxygène. Un hydrocarbure est un un groupe de composés, comme le nom l'indique contenant des atomes d'hydrogène et de carbone. Parmi les hydrocarbures, nous entendons souvent parlé de méthane (gaz à effet de serre), le butane (essence à briquet), le propane (carburant commun des BBQ) et l'octane (carburant des automobiles). La formule générale d'une combustion complète suit l'équation :
Souvent, une combustion est incomplète et produira également du monoxyde de carbone (CO), un composé très toxique qui est surnommé le « tueur silencieux » en raison des décès qu'il occasionne dans les maisons qui ont un système de chauffage par combustion et que l'échappement des gaz n'est pas bien ventilé à l'extérieur de la maison.
Exemples de combustion : combustion du 1) méthane CH4 et 2) du propane C3 H8
Ressources
Tableau périodique interactif des indices d'électronégativité sur elementschimiques.fr
| Fiche sur le nombre d'Avogadro | |
| File Size: | 236 kb |
| File Type: | |
Réactifs limitants et rendement d'une réaction sur Khanacademy