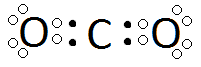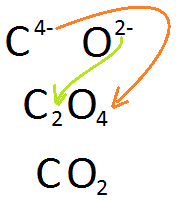L’élève sera apte à :
- expliquer la correspondance entre la position d'un élément dans le tableau périodique et sa capacité de combinaison (valence), entre autres les métaux alcalins, les alcalinoterreux, les chalcogènes, les halogènes, les gaz rares;
- expliquer, au moyen du tableau périodique, comment et pourquoi les éléments se combinent les uns avec les autres dans des proportions particulières, entre autres les liaisons ioniques et les liaisons covalentes, la formation de composés;
- écrire la formule et le nom de composés ioniques binaires, entre autres respecter les lignes directrices de l'Union internationale de chimie pure et appliquée (UICPA) et justifier leur utilisation;
- écrire, en utilisant des préfixes, la formule et le nom de composés covalents (moléculaires), entre autres mono-, di-, tri-, tétra-;
Configuration électronique - Lewis
Les atomes ont tendance à rechercher des couches de valence complète. Pour y arriver, ils ont besoins d'obtenir des électrons manquant ou de perdre des électrons en trop. Lorsque deux atomes entre en contacts, avec de l'énergie, ils peuvent s'échanger des électrons en créant une liaison entre eux. Pour bien représenter les besoins de liaison des atomes, on les représentent souvent avec seulement leur couche de valence (leur dernière couche). On appelle cette représentation la « structure de Lewis » en l'honneur du physicien américain Gilbert Newton Lewis. À titre d'exemple, voici quelques exemple de représentation de Bohr et de structure de Lewis correspondante pour quelques atomes :
|
Les schémas de Bohr montre le nombre d'électrons sur chaque niveau d'énergie alors que dans la structure de Lewis, on ne représente que les électrons de la couche supérieure. Ce sont ces électrons qui donnent à l'atome ses propriétés chimiques de liaisons.
Le carbone possède 4 électrons de valence. Il y a donc 4 électrons représentés dans la structure de Lewis. Le carbone doit obtenir 4 autres électrons pour compléter sa couche de valence. L'oxygène possède 6 électrons de valence. On place les électrons par couple sur chaque côté du symbole de l'élément. L'oxygène peut donc obtenir 2 électrons pour compléter sa couche. |
En neuvième année, nous avons vu comment dessiner les configurations électroniques de Bohr pour les 18 premiers éléments. La configuration suivait une règle simple :
- Les deux premiers électrons sur la première couche;
- Les huit électrons suivants sur la seconde couche;
- Les huit électrons suivants sur la troisième couche.
Modèle quantique
La théorie de Bohr, datant de 1913, est satisfaisante pour les premiers éléments, mais elle ne permet pas d'expliquer la configuration électronique des suivants. Les recherches sur l'atome se sont poursuivit après le modèle de Bohr. C'est vers 1925 que le modèle quantique est apparu.
Selon ce modèle, une particule comme l'électron est caractérisée par quatre paramètres : les quatre nombres quantiques n, l, m, s.
- n est le nombre quantique principal; il correspond au numéro de la couche électronique.
- l est le nombre quantique secondaire ou le nombre quantique azimutal, il se définit par rapport à n : l est un nombre entier positif qui peut prendre les valeurs comprises en 0 et n - 1. Chaque valeur porte un nom désigné par une lettre minuscule :
Valeur 0 1 2 3 4
Nom s p d f g
Il correspond à la sous-couche. - m est le nombre quantique magnétique. Il se définit par rapport à l : m est un nombre entier qui peut prendre (2.l + 1) valeurs encadrées en l et -l :
Pour l = 0 : m = 0,
pour l = 1 : m = -1 ou m = 0 ou m = 1,
pour l = 2 : m = -2 ou m = -1 ou m = 0 ou m = 1 ou m = 2,
etc.
Ce nombre traduit l'orientation de l'orbitale dans un champ magnétique. - s est le nombre quantique de spin. Dans le cas de l'électron, il peut prendre les valeurs 1/2 représenté par une flèche pointant vers le haut et -1/2 représenté par une flèche pointant vers le bas, conséquence de la rotation de l'électron sur lui-même.
|
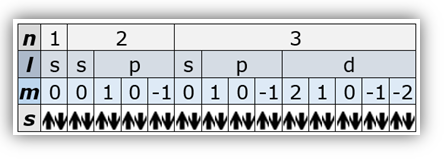
Orbitales
A chaque valeur de (n, l, m, s) correspond une orbitale atomique (voir tableau) Une orbitale est notée par la valeur de n suivi du nom de la sous-couche. Ainsi l'orbitale 2p correspond à n = 2 et l = 1. Il y a 6 orbitales possibles sur une orbitale atomique (OA) de type p, correspondant aux 3 valeurs de m x 2 valeurs de s. |
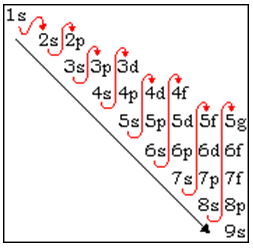
Pour simplifier, On peut utiliser le tableau à droitepour trouver le nombre d'électron sur chaque orbitale.
- On commence par remplir la sous-couche 1s qui peut contenir 2 électrons. Ceci explique pourquoi il n'y a que deux électrons sur la première couche : le nombre n=1 ne contient qu'une seule orbitale, s, qui ne peut accueillir que deux électrons.
- On remplit ensuite l'orbitale 2s qui contient 2 électrons, puis on passe à 2p qui peut en contenir 6. Cela explique pourquoi le niveau n=2 contient un maximum de 8 électrons.
- On passe ensuite à 3s (2 électrons), puis 3p (6 électrons).
- On remplit ensuite la sous-couche 4s (2 électrons). Jusqu'à maintenant, on a suivi les mêmes règles que pour le modèle de Bohr avec n=1 (2 électrons), n=2 (8 électrons), n=3 (8 électrons), n=4 (2 électrons).
- Maintenant, on poursuit en retournant à la couche n=3 avec l'orbitale 3d qui peut contenir jusqu'à 10 électrons (correspondant aux éléments des métaux de transition (scandium à zinc)
- Les électrons suivants se placent sur l'orbitale 4p qui contient un maximum de 6 électrons.
- Et ainsi de suite...
1s2 2s2 2p6 3s2 3p6 4s2 3d6
On remarque que l'orbite n le plus élevé est l'orbite 4 avec 2 électrons. Le fer possède donc 2 électrons de valence. Un deuxième exemple permet de mieux comprendre.
configuration électronique de l'iode (53 électrons) : 1s2 2s2 2p6 3s2 3p6 4s2 3d10 4p6 5s2 4d10 5p5.
n=5 est le niveau le plus élevé. Avec 2 sur 5s et 5 sur 5p, l'iode possède 7 électrons de valence.
Il faut ajouté 4 électrons de valence d'une orbitale à la suivante
- 2 électrons sur s
- 6 électrons sur p
- 10 électrons sur d
- 14 électrons sur f (série des lanthanides et des actinides)
- 18 électrons sur g
Exceptions
Cette règles de remplissage fonctionne bien pour la plupart des éléments. Toutefois, certains éléments, peu nombreux, ne suivent pas la règle. Le chrome et le cuivre font partie de ces exceptions.
Pour dessiner la structure de Lewis des éléments, il suffit de compter le nombre d'électrons se trouvant sur le nombre n le plus élevé dans la configuration électronique de l'atome de l'élément. Si on a de la difficulté à établir la configuration électronique, il existe des tableaux périodiques qui les fournissent.
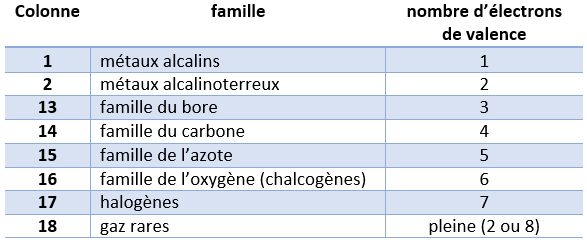
Famille d'éléments - capacité de combinaison
La position d'un atome dans le tableau périodique détermine donc sa tendance à gagner ou à perdre des électrons.
Où est-ce que les atomes trouvent les électrons qui leur manquent? À quel endroit est-ce que les atomes peuvent se débarrasser des électrons qu'ils ont en trop? La réponse à ces deux questions est la même : chez d'autres atomes.
Liaisons ioniques
De manière générale, un composé ionique est un composé formé d'un métal et d'un non-métal.
Formule chimique d'un composé ionique
Pour chaque atome de lithium, il faut un atome de fluor pour que les deux atomes complètent leur couche de valence. Il y a donc un rapport de 1 pour 1 qui est représenté par la formule du composé LiF. Le lithium qui perd son électron obtient une charge de 1+ et le fluor qui gagne un électron obtient une charge de 1-. Le LiF est donc composé de deux ions le Li+ et le F-.
La formule chimique s'écrit s'écrit toujours en commençant par l'ion positif suivi de l'ion négatif.
Voici quelques exemples de composés ioniques binaires (deux éléments) suivant la même logique :
L'iodure de potassium est composé de potassium et d'iode. Le potassium est un alcalin avec un électron de valence et l'iode est un halogène avec 7 électrons de valence. L'iode capte l'électron du potassium pour compléter sa couche de valence. Il devient un ion I-. Le potassium qui cède son électron devient un ion K+. La formule chimique est donc le KI.
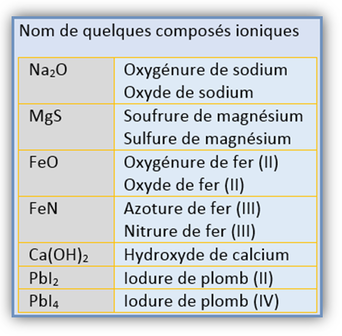
L'oxyde de sodium est composé d'oxygène et de sodium. L'oxygène possède 6 électrons de valence. Il aura donc besoin de 2 électrons pour compléter sa couche de valence et devenir un ion O2-. Le sodium, avec 1 électron de valence, cherchera à s'en débarrasser pour devenir un ion Na+. Il faudra donc deux ions Na+ pour fournir deux électrons à l'ion O2-. La formule chimique de l'oxyde de sodium est le Na2O.
Le chlorure de calcium est composé de chlore et de calcium. Le chlore possède 7 électrons de valence. Il aura donc besoin de 1 électron pour compléter sa couche de valence et devenir un ion Cl-. Le calcium, avec 2 électrons de valence, cherchera à s'en débarrasser pour devenir un ion Ca2+. Il faudra donc deux ions Cl1 pour accepter deux électrons de l'ion Ca2+. La formule chimique du chlorure de calcium est le CaCl2.
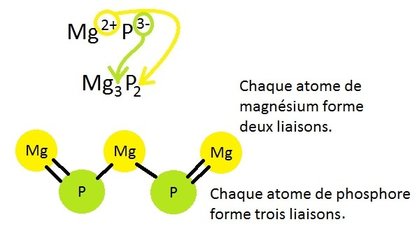
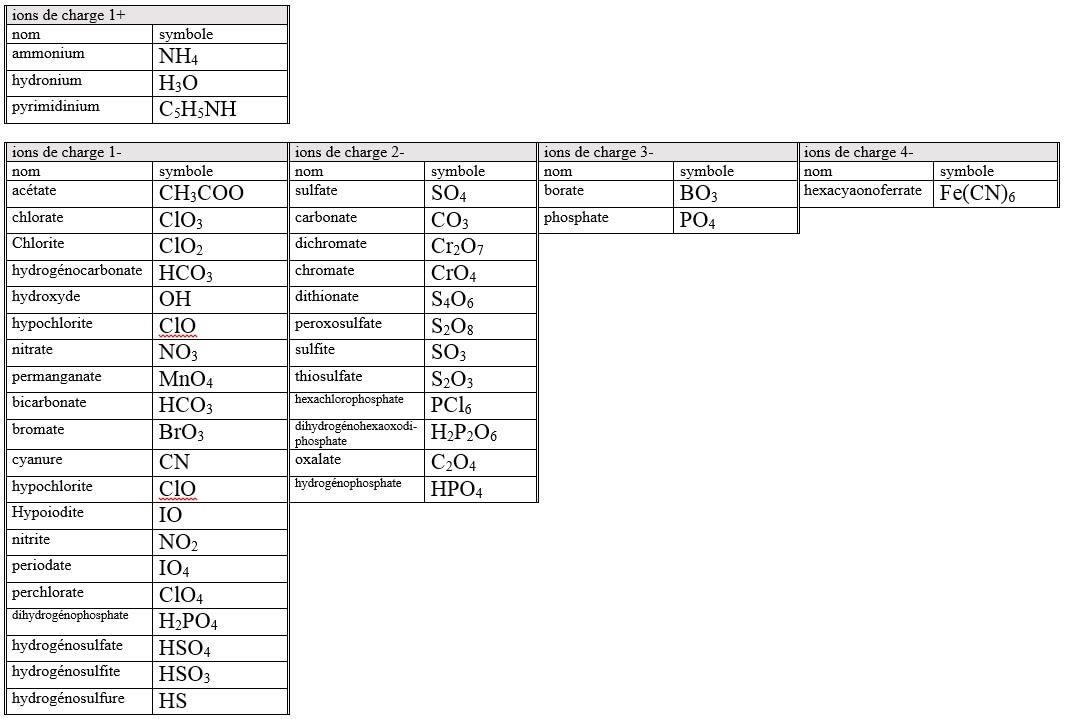
Ions polyatomiques
Le sulfate de potassium est composé de l'ion potassium K+ et d'ion sulfate SO42-. Par la même logique que pour les liaisons binaires, il faudra 2 ions K+ pour chaque ion SO42-. La formule du sulfate de potassium est donc le K2SO4.
L'hydroxyde de calcium est composé de l'ion calcium Ca2+ et d'ion hydroxyde OH-. Il faudra 2 ions OH- pour chaque ion Ca2+. La formule de l'hydroxyde de calcium est le Ca(OH)2. Dans ce cas, pour montrer que l'indice 2 est attribué à l'ion OH, on ajoute des parenthèses.
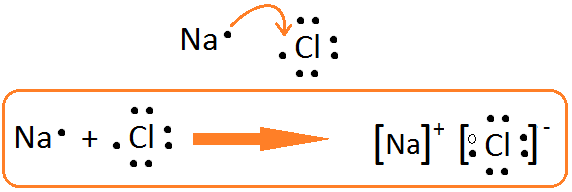
Représentation d'une liaison ionique par la structure de Lewis
|
En haut, on montre que l'électron de valence du sodium passe à l'atome de chlore. En bas, dans le cadre, on montre la réaction chimique sous forme d'équation avec la notation de Lewis. La liaison entre les atomes de sodium et de chlore est représenté à droite de l'équation par l'ion Na+ lié à l'ion Cl-. Les deux ions sont entre crochets et l'électron du sodium est représenté par un cercle vide autour du symbole du chlore. Les niveaux d'oxydation sont représentés par les charges + et - en exposant.
|
Liaisons covalentes
Il existe un autre type de liaison où les atomes ne donnent pas d'électrons, mais les partagent. Il s'agit de liaisons covalentes. En général, ces liaisons se produisent entre deux atomes qui forment normalement des ions négatifs (deux atomes non métalliques par exemple).
Pour illustrer ce type de liaison, prenons l'exemple du dioxyde de carbone composé des deux non-métaux que sont le carbone et l'oxygène, formant normalement des ions C4- et O2-. Le carbone cherche à compléter sa couche de valence en obtenant 4 électrons. L'oxygène, quant à lui, cherche à obtenir 2 électrons. Puisque les deux atomes cherchent à prendre des électrons de l'autre, il ne peut y avoir un atome qui donne et l'autre qui reçoit les électrons. Les deux atomes vont alors partager des électrons qu'ils mettent en commun pour les deux atomes. Le carbone met en commun 4 électrons et l'oxygène 2. chaque électron mis en commun par un atome doit se trouver en pair avec un électron mis en commun par l'autre atome. Il faudra 2 atomes d'oxygène pour chaque atome de carbone afin que cette règle soit respectée. Le CO2 est formé. Lorsque les deux atomes partagent ainsi des électrons, on dit que le composé est covalent.
|
Indice d'électronégativité
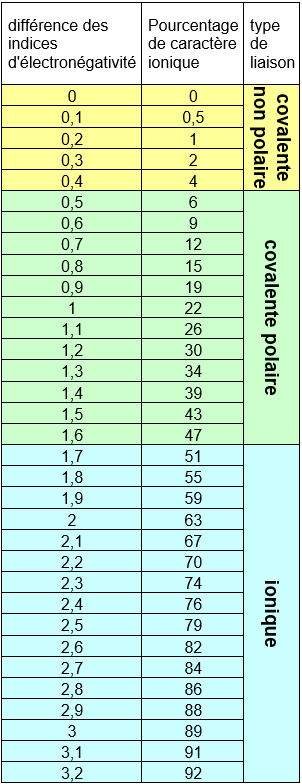
Comment savoir l'ordre des symboles dans la formule des composés covalents puisque les deux niveaux d'oxydation sont négatifs? En règle général, les éléments qui se trouve plus à gauche dans le tableau périodique se retrouve aussi à gauche dans la formule chimique. Mais ce n'est pas une règle absolue. En réalité, l'élément qui attire le plus les électrons (le plus négatif) est à droite dans la formule. Pour savoir quel élément attire le plus les électrons, on trouve l'indice d'électronégativité de l'élément. Ces indices sont donnés dans plusieurs tableaux périodiques. Le carbone a un indice d'électronégativité de 2,55. L'oxygène a un indice de 3,44. L'oxygène attirera plus les électrons que le carbone et on l'écrit à droite dans la formule. Par définition, un composé est covalent si la différence des indices d'électronégativité entre ses ions est inférieure ou égale à 1,6. Le tableau à droite montre le pourcentage de caractère ionique de liaisons selon la différence d'électronégativité entre les ions. La différence d'électronégativité entre le carbone et l'oxygène est de 0,89 (3,44-2,55). Selon le tableau, le dioxyde de carbone est donc un composé covalent polaire avec un pourcentage de caractère ionique d'environ 19%. Un composé covalent polaire signifie que même si les deux ions se partagent des électrons, l'ion oxygène tire plus fortement les électrons que l'ion carbone. Ceci crée un léger déséquilibre dans les charges et la molécule aura tendance à être légèrement négative près de l'oxygène et légèrement positive près du carbone. Le dioxyde de carbone est donc légèrement «polarisé». |
Nomenclature
Composé ionique
- on donne le nom de l'ion négatif en premier. S'il s'agit d'un ion monoatomique, on ajoute le suffixe -ure à la fin du nom (fluor devient fluorure, brome devient bromure, etc.). On peut toujours suivre cette règle, mais certains éléments portent des noms différents. Voici les exceptions :
- Carbone : carbure
- Azote : nitrure
- Oxygène : oxyde
- Phosphore : phosphure
- Soufre : sulfure
- Sélénium : séléniure
- On poursuit avec le nom de l'ion positif précédé du mot «de».
- Dans le cas d'ons positifs possédant plusieurs niveaux d'oxydations possible, on ajoute le niveau d'oxydation en chiffres romains entre parenthèse (on retrouve aussi des notations sans parenthèses)
(Dans les cas d'exception, on donne le nom selon la règle de base et ensuite le nom qui est plus correct)
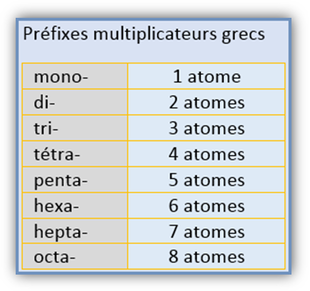
Pour les composés covalents, il faut d'abord connaître les préfixes grecs représentant les multiples. Voici un tableau des 8 premiers préfixes de multiplication.
|
Ressources
| composés_covalents.pdf | |
| File Size: | 223 kb |
| File Type: | |
| Les composés chimiques et les liaisons | |
| File Size: | 1324 kb |
| File Type: | |
| les_composés_ioniques_-_exercice_-_solution.pdf | |
| File Size: | 147 kb |
| File Type: | |