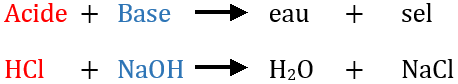L’élève sera apte à :
- mener des expériences pour classer des acides et des bases selon leurs propriétés particulières, entre autres le pH, les indicateurs, la réactivité en présence de métaux;
- discuter de la manifestation d'acides et de bases dans des systèmes biologiques,des processus industriels et des applications domestiques,entre autres tenir compte des effets sur l'environnement, la sécurité et la santé;
- expliquer comment un acide et une base interagissent pour former un sel et de l'eau au cours du processus de neutralisation;
Qu'est-ce qu'un acide ou une base?
Arrhenius
Le suédois Svante August Arrhenius a donné les définitions suivantes :
- Un acide est une substance qui en solution aqueuse, libère un ou plusieurs protons (H+) ;
- Une base est une substance qui en solution aqueuse libère un ou plusieurs ions OH- ;
- La réaction acide-base est une réaction où il y a formation d'eau (liaison entre 0H- et H+) et de sel.
Brønsted-Lowry
Les chimistes anglais Thomas Lowry et danois Joannes Brønsted ont présenté des définitions différentes. Selon Brønsted, la réaction d'un acide ou d'une base entraîne un transfert de proton (H+) de l'un des deux composés vers l'autre :
- Un acide est une espèce chimique qui a tendance à céder un ou plusieurs protons (ion H+) ;
- Une base est une espèce chimique qui a tendance à capter un ou plusieurs protons ;
- La réaction acide-base est un transfert de H+ (proton) entre deux couples acides-bases.
Lewis
L'américain Gilbert Newton Lewis apporte une autre définition :
Un acide est toute espèce qui peut accepter une paire d'électrons offerte par une autre espèce chimique lors d'une réaction. Un acide de Lewis est un accepteur d'électrons (électrophile).
Une base est une espèce qui possède une paire d'électron non-liante et qui peut offrir une paire d'électrons à une autre espèce chimique lors d'une réaction. Une base de Lewis est donc un donneur d'électrons.
Dans le cours de sciences de la nature 20F, nous étudierons des acides et bases particulières répondant aux définitions suivantes :
Acide : Un acide est une substance composée d'ion H+ et d'un ion non métallique- en solution liquide.
Base : Une base est une substance composée d'un ion métallique+ et d'un ion hydroxyde OH-.
Exemples d'acides et de bases suivants ces définitions :
HCl : acide chlorhydrique composé de l'ion H+ et de l'ion Cl-
H2SO4 : acide sulfurique composé de l'ion H+ et de l'ion polyatomique SO42-
Base
NaOH : hydroxyde de sodium composé de l'ion OH- et de l'ion Na+
Mg(OH)2 : hydroxyde de magnésium composé de l'ion OH- et de l'ion Mg2+
Caractéristiques des acides et des bases
- Ils ont un goût sûr (comme l'acide des citrons ou des oranges)
- Ils sont corrosifs et réagissent avec les métaux pour dégager de l'hydrogène et un composé ionique soluble.
- Ils colorent le papier tournesol vers le rouge
- Ils ont un pH < 7
- Elles ont un goût amer (comme le lait de magnésie)
- Elles sont corrosives pour les tissus organiques comme la peau (exemple : eau de javel ou hypochlorite de sodium NaClO)
- Elles ont une texture savonneuse, glissante
- Elles colorient le papier tournesol vers le bleu
- Elles ont un pH > 7
L'eau est neutre. Il n'est ni un acide, ni une base. son pH est de 7. l'eau est à la fois composé de l'ion H+ et de l'ion OH-.
Nomenclature des acides et bases simples
Les acides binaires (comportant deux éléments différents) que nous étudions dans ce cours sont formés d'un ion H+ et d'un ion non métallique négatif. Leur nomenclature suivent les règles suivantes :
Nous aurons par exemple les acides suivants :
HClaq : acide chlorhydrique (formé de l'ion non-métallique chlore)
HFaq : acide fluorhydrique (formé de l'ion non-métallique fluor)
H2Saq : acide sulfurhydrique (formé de l'ion non-métallique soufre)
H3Paq : acide phosphorhydrique (formé de l'ion non-métallique phosphore)
La nomenclature des bases hydroxydes que nous étudions dans ce cours ne diffère pas de la nomenclature des composés ioniques. On suit donc la règles suivantes :
Nous aurons par exemple les bases suivantes :
NaOHaq : hydroxyde de sodium (formé de l'ion métallique Na+)
Ca(OH)2 aq : hydroxyde de calcium (formé de l'ion métallique Ca2+)
Mg(OH)2 aq : hydroxyde de magnésium (formé de l'ion métallique Mg2+)
Fe(OH)3 aq : hydroxyde de fer III (formé de l'ion métallique Fe3+)
pH
Le pH est une mesure du taux d'acidité d'une solution. pH signifie puissance d'hydronium ou potentiel hydrogène. l'hydronium est l'ion H3O+. Il correspond à de l'eau H2O auquel est ajouté un ion H+. L'eau pur contient une concentration de 10-7 mole d'ion H3O+ par litre d'eau. Le pH de l'eau est donc de 7.
Comme expliqué dans la définition des acides un ion H+ est libéré par un acide en solution aqueuse. Ceci a pour effet d'augmenté la concentration d'ions H3O+ dans l'eau, réduisant le pH. Par exemple, l'acide chlorhydrique concentré peut atteindre un pH inférieur à 1, soit une concentration en ions H3O+ supérieure à 10-1 mole de H3O+ par litre d'eau
Les bases ont l'effet inverse des acides. Les ion OH- libérées par les bases s'associent avec les ions H3O+ de l'eau pour former des molécules d'eau H2O. Ceci a pour effet de réduire la concentration en ions H3O+ de l'eau qui augmentra le pH. Par exemple, l'eau de javel concentré atteint un pH de 12,5. Ceci correspond à une réduction de la concentration de H3O+ dans l'eau à un niveau de 10-12,5 (ou 3,16 x 10-13 mole de H3O+ par litre d'eau.
En résumé, le pH correspond à la valeur absolue de l'exposant de la concentration de H3O+ en mole par litre d'eau.
Neutralisation
Utilisation des acides et des bases
Plusieurs des premiers européens à passer l'hiver au Canada ont souffert du scorbut, une maladie grave qui causa la mort de 25 des 110 hommes d'équipage de la deuxième expédition de Jacques Cartier. L'origine de cette maladie est une carence en vitamine C qu'on retrouve dans plusieurs aliments végétaux comme les fruits et les légumes. L'hiver canadien ne permettait pas aux explorateurs européens la culture de ces denrées et on ignorait, avant les conseils de Domagaya, fils du chef nadouek-iroquoien Donnacona, d'autres sources alimentaires de la vitamine.
La vitamine C est le nom commun donné à l'acide ascorbique (acide antiscorbutique). Cette substance joue un rôle important dans le corps humain et dans celui de nombreux animaux. L'acide ascorbique n'est pas le seul composé acide ou basique à contribuer au métabolisme du corps. Le sang, lui-même, a un pH doit devant demeurer entre 7,38 et 7,42. L'ADN des chromosomes est un acide, contenant également des bases azotées, et utilise des acides aminées pour fabriquer les protéines nécessaires à la vie. Les acides gras sont utilisés par le corps comme source d'énergie où l'acide phosphorique contribue à la création des molécules d'ATP (molécule énergétique).
Le suc gastrique est le liquide de l'estomac qui permet la digestion des aliments. Son pH avoisine le 2. Il est composé principalement d'acide chlorhydrique. Lorsqu'il y a un excès d'acide dans l'estomac, le pH diminue et suivent les brûlures d'estomac. Les médicaments antiacides peuvent alors aider à neutraliser l'acidité. Les antiacides sont des bases. On les retrouve habituellement sous forme de lait de magnésie (hydroxyde de magnésium) ou en capsule combiné avec du carbonate de calcium.
Les savons sont aussi généralement composés de bases faibles qui permettent la dissolution des matières grasses. Et, si vous avez des maux de tête, l'aspirine (acide acétylsalicylique) est souvent la solution.
Utilisation des acides et des bases dans les processus industriels.
Les acides et les bases sont très utilisés dans l'industrie. L'acide sulfurique, par exemple, sert à la production d'engrais, au décapage des métaux, au traitement des eaux usés, à la fabrication d'explosifs, au raffinage de pétrole, etc. C'est sans doute l'acide le plus utilisés dans l'industrie.
L'ammoniac est sans doute la base la plus utilisée dans l'industrie. On l'utilise dans la fabrication d'engrais, d'explosifs, de polymères (matières plastiques, caoutchouc, colles, peintures, résines, ...), dans la fabrication des cigarettes. On l'utilise aussi comme agent réfrigérant dans les réfrigérateurs industriels. À cause de son odeur forte et facilement identifiable, on l'a aussi utilisé dans la détection des fuites.
Utilisation domestique des acides et des bases.
Que ce soit pour déboucher des tuyaux ou pour nettoyer les fenêtres, les acides et les bases entrent dans la composition de nombreux produits ménagers. Les savons de lessive sont habituellement alcalines (plusieurs contenant des phosphates). On nettoie aussi la rouille avec des acides : L'acide phosphorique réagit avec la rouille de fer pour former du phosphate de fer qui protège le métal. Les batteries de nos automobiles utilisent l'acide sulfurique comme électrolyte.
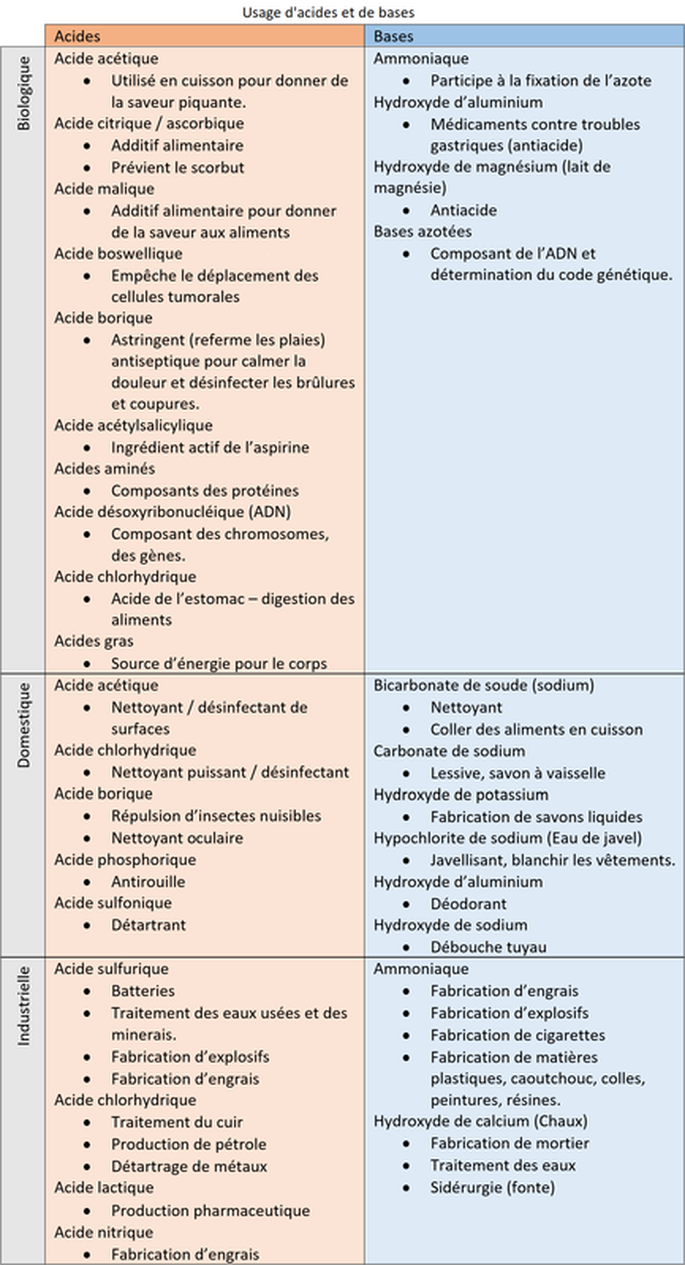
Le tableau suivant résume quelques usages d'acides et bases.
Ressources
| Article du magazine La recherche de juin 2008 | |
| File Size: | 2154 kb |
| File Type: | |